Yuanfeng POV: Обновленный график EUDAMED
Недавно Комиссия ЕС объявила об обновлениях для завершения и реализации EUDAMED на основе поправки 2024/1860.В этой статье изложены текущие графики EUDAMED и наша точка зрения на эти графики, чтобы помочь промышленности подготовиться соответственно.
Текущие графики EUDAMED:
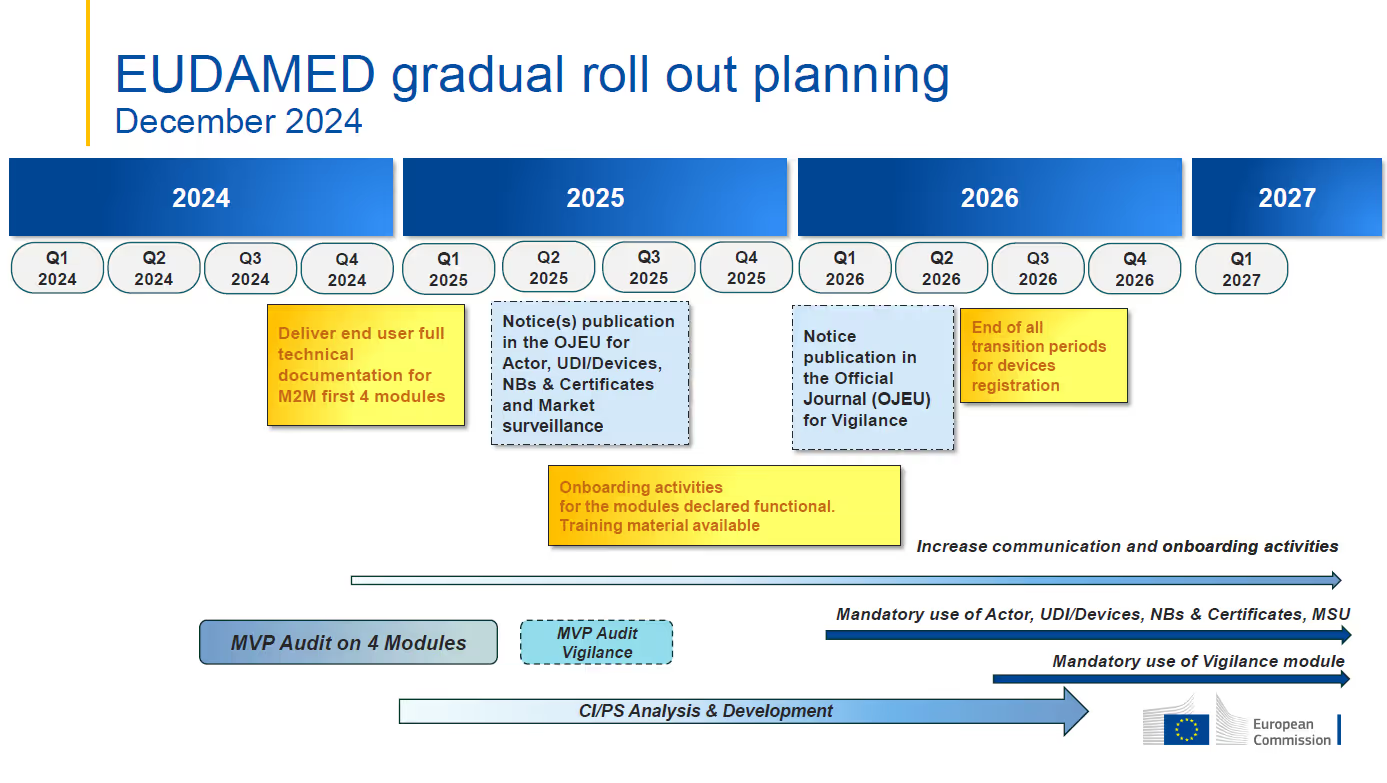
- Целевая дата первого обязательного применения функциональных модулей EUDAMED по-прежнему составляет 1 января 2026 года.Ожидается, что модуль бдительности станет обязательным с 3 квартала 2026 года, а полная функциональность EUDAMED планируется в 2 квартале 2027 года..
- В настоящее время проверяются модули Actor, UDI & Devices, Certificates и Market Surveillance.Независимый аудит минимального жизнеспособного продукта (MVP) предназначен для оценки и подтверждения функциональности и взаимосвязанности модулей, которые считаются готовыми к аудиту.Этот аудит должен быть завершен к второму кварталу 2025 года.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Ожидается, что модули актера, UDI & Devices, сертификатов и мониторинга рынка будут объявлены полностью функциональными в конце второго квартала 2025 года, что приведет к их обязательной дате применения 1 января. 2026.
- Что? - Ожидается, что модули Actor, UDI & Devices, Certificates и Market Surveillance будут объявлены полностью функциональными к концу второго квартала 2025 года и обязательными для промышленного использования 1 января 2026 года.
- Модуль слежки не является частью текущего аудита MVP и не будет объявлен полностью функциональным вместе с ранее упомянутыми модулями.Пересмотренный график указывает, что аудит этого модуля состоится между II и III кварталом 2025 года., с целью обязательной даты применения во втором квартале 2026 года.
- Что? - Разработка модуля "Клинические исследования/исследования эффективности" (CI/PS) должна продолжаться до третьего квартала 2026 года.Аудит для оценки модуля CI/PS вместе с другими пятью (5) модулями будет завершен после разработки MVP CI/PS.
- Что?
Фотография предоставленаЕвропейская комиссия
Европейская комиссия недавно объявила об обновлениях для завершения и внедрения EUDAMED на основеПоправка 2024/1860.В этой статье изложены текущие графики EUDAMED и наша точка зрения на эти графики, чтобы помочь промышленности подготовиться соответственно.
Текущие графики EUDAMED:
- Целевая дата первого обязательного применения функциональных модулей EUDAMED по-прежнему составляет 1 января 2026 года.Ожидается, что модуль бдительности станет обязательным с 3 квартала 2026 года, а полная функциональность EUDAMED планируется в 2 квартале 2027 года..
- В настоящее время проверяются модули Actor, UDI & Devices, Certificates и Market Surveillance.Независимый аудит минимального жизнеспособного продукта (MVP) предназначен для оценки и подтверждения функциональности и взаимосвязанности модулей, которые считаются готовыми к аудиту.Этот аудит должен быть завершен к второму кварталу 2025 года.
- Mandatory use of each module is to commence six (6) months after the module is declared fully functional through the independent audit and publication in the Official Journal of the European Union (OJEU)Ожидается, что модули актера, UDI & Devices, сертификатов и мониторинга рынка будут объявлены полностью функциональными в конце второго квартала 2025 года, что приведет к их обязательной дате применения 1 января. 2026.
- Что? - Ожидается, что модули Actor, UDI & Devices, Certificates и Market Surveillance будут объявлены полностью функциональными к концу второго квартала 2025 года и обязательными для промышленного использования 1 января 2026 года.
- Модуль слежки не является частью текущего аудита MVP и не будет объявлен полностью функциональным вместе с ранее упомянутыми модулями.Пересмотренный график указывает, что аудит этого модуля состоится между II и III кварталом 2025 года., с целью обязательной даты применения во втором квартале 2026 года.
- Что? - Разработка модуля "Клинические исследования/исследования эффективности" (CI/PS) должна продолжаться до третьего квартала 2026 года.Аудит для оценки модуля CI/PS вместе с другими пятью (5) модулями будет завершен после разработки MVP CI/PS.
- Что?

Фотография предоставленаЕвропейская комиссия
Вот как Rimsys рассматривает влияние этого объявления для каждой группы заинтересованных сторон:
Юаньфэн
УДИ - это наше главное направление, а также будущее взаимодействие с модулем бдительности.поскольку Rimsys продолжит развивать функциональность UDI и пострыночного надзора независимо от обновленных целевых датМы также признаем потенциальное влияние создания возможностей передачи данных (DTX) для взаимодействия с EUDAMED в качестве машины-машине (M2M).С публикацией окончательных требований, необходимых для M2M DTX для EUDAMED, Rimsys находится в позиции, чтобы завершить наше соединение и предоставить возможности M2M в рамках решения EUDAMED.
Промышленность/заказчик
Поскольку Европейская комиссия (EC) неоднократно обновляла сроки EUDAMED, мы ожидаем, что промышленность будет не очень охотно принимать новые целевые даты.Это может задержать повторное участие в подготовке EUDAMED.Однако мы не ожидаем, что ЕС продлит эти обновленные сроки.Производители, которые не планируют предоставлять данные EUDAMED к II кварталу этого года, должны ожидать значительных проблем для достижения этих сроков.В настоящее время проводится аудит ожидаемых модулей и опубликована соответствующая техническая документация.Rimsys рекомендует предпринять шаги для организации регуляторных данных сейчас и предоставления их информации в раннем возрасте во все доступные модули EUDAMED.
Европейская комиссия
ЕС настоятельно рекомендует промышленности продолжать разработку своего решения и предоставлять данные на добровольной основе.Позиция Комиссии заключается в том, что предоставление данных в раннем периоде дает компаниям преимущество, поскольку их данные будут доступны до наступления всей мировой индустрии медико-технологий.Эти компании также будут впереди, чтобы работать с ресурсами комиссии, если возникнут проблемы с представлением данных.
* Примечание - в данной статье содержатся регуляторные интерпретации и мненияЮаньфэнМы стараемся быть максимально информативными, но эта информация не предназначена для замены официальных рекомендаций регулирующих органов.

